Artykuł Jak powstaje blizna i jakie są rodzaje?
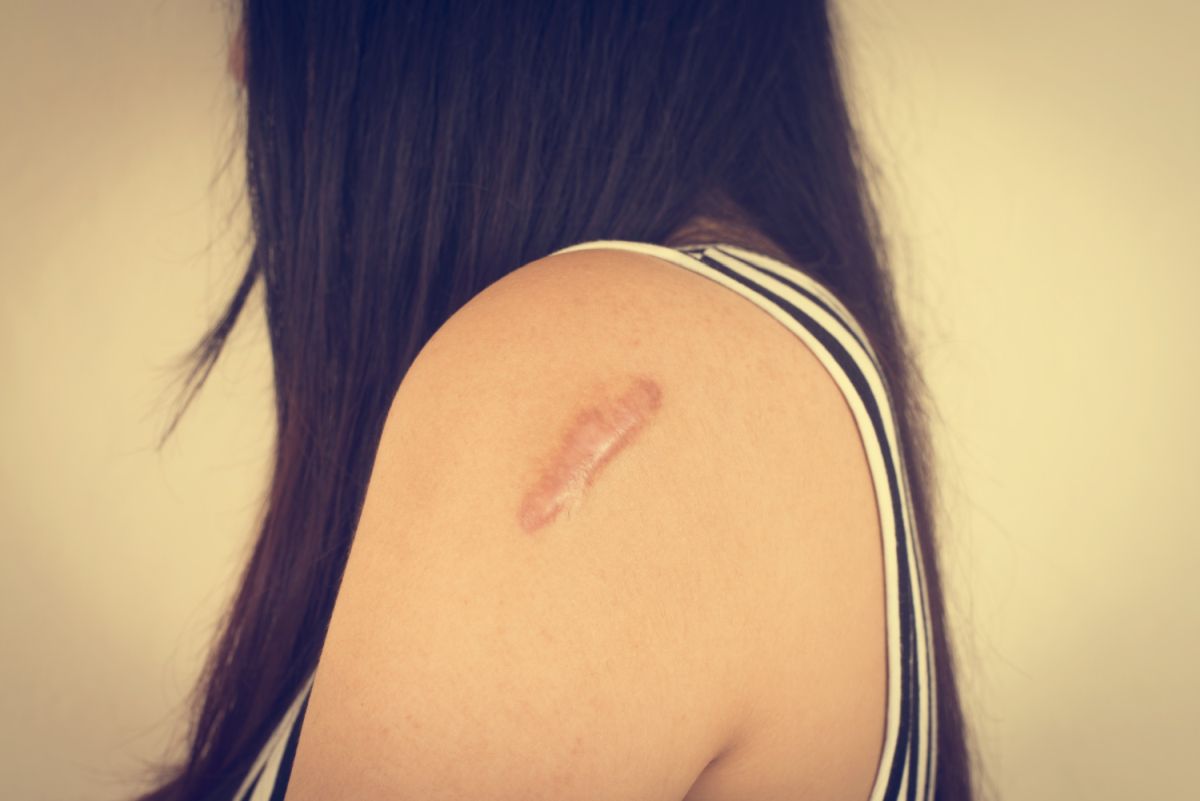
Jak powstaje blizna i jakie są rodzaje?
TL;DR
-
Proces gojenia rany i formowania blizny dzieli się na trzy fazy: zapalną (do 72 godzin), proliferacyjną (do 15 dni) i remodelingu (do 2 lat).
-
Blizna początkowo ma czerwone zabarwienie z powodu tworzenia się nowych naczyń krwionośnych w procesie angiogenezy.
-
Wyróżnia się blizny prawidłowe, zanikowe (atroficzne), przerosłe (hipertroficzne) oraz bliznowce (keloidy).
-
Bliznowce, w odróżnieniu od blizn przerosłych, rozrastają się poza granice pierwotnego uszkodzenia skóry.
Blizna jest strukturą tkanki łącznej włóknistej, która powstaje w miejscu uszkodzenia skóry lub tkanki.
Co to jest blizna skórna?
Blizna skórna stanowi trwałą zmianę, w której uszkodzona skóra właściwa zostaje zastąpiona przez tkankę łączną włóknistą. Jej głównym budulcem jest kolagen, przede wszystkim typu I i III, jednak w proporcjach odmiennych niż w zdrowej skórze, gdzie dominuje kolagen typu I. Włókna kolagenowe w bliźnie układają się równolegle do powierzchni skóry, w przeciwieństwie do siateczkowatej struktury w tkance prawidłowej. Ta zdezorganizowana architektura jest bezpośrednią przyczyną mniejszej elastyczności i odmiennej tekstury blizny.
Struktura blizny jest pozbawiona fizjologicznych przydatków skórnych, takich jak mieszki włosowe, gruczoły łojowe oraz potowe. Brak gruczołów łojowych uniemożliwia produkcję sebum, co skutkuje brakiem naturalnego nawilżenia i natłuszczenia powierzchni blizny. Z kolei nieobecność gruczołów potowych upośledza lokalną zdolność do termoregulacji poprzez wydzielanie potu. Tkanka bliznowata często ma również zmniejszoną liczbę melanocytów, co powoduje jej jaśniejszy kolor i brak zdolności do opalania.
Proces tworzenia blizny, zwany bliznowaceniem, jest biologicznym mechanizmem naprawczym organizmu, którego celem jest szybkie zamknięcie rany. Priorytetem tego procesu jest przywrócenie bariery ochronnej skóry, a nie odtworzenie jej pierwotnej, złożonej struktury. Bliznowacenie jest końcowym etapem gojenia, następującym po fazach hemostazy, zapalenia i proliferacji. Ostateczny wygląd blizny kształtuje się podczas ostatniej fazy, zwanej przebudową lub remodelingiem, która może trwać od kilku miesięcy do nawet dwóch lat.
Jak przebiega proces gojenia rany?
Proces gojenia rany jest złożonym mechanizmem biologicznym, obejmującym cztery sekwencyjne, lecz nakładające się na siebie etapy gojenia blizny: hemostazę, zapalenie, proliferację oraz remodeling. Faza hemostazy, inicjowana bezpośrednio po przerwaniu ciągłości naczyń krwionośnych, ma na celu natychmiastowe zatrzymanie krwawienia i trwa od kilku minut do kilku godzin. rolę odgrywa w niej agregacja płytek krwi, które przylegają do uszkodzonego śródbłonka, oraz aktywacja kaskady krzepnięcia, prowadząca do przekształcenia fibrynogenu w nierozpuszczalny włóknik. Uformowany w ten sposób skrzep fibrynowy nie tylko zamyka ranę, ale również stanowi macierz dla migracji komórek zapalnych i fibroblastów w kolejnych fazach.
Faza zapalna rozpoczyna się w ciągu kilku godzin od urazu i osiąga szczyt w ciągu 24-72 godzin, a jej celem jest oczyszczenie rany z drobnoustrojów i martwych tkanek. Wzrost przepuszczalności naczyń krwionośnych umożliwia migrację do rany komórek układu odpornościowego, w pierwszej kolejności neutrofili. Neutrofile, dominujące w ranie przez pierwsze 2-3 dni, prowadzą fagocytozę bakterii i uwalniają enzymy proteolityczne. Po nich pojawiają się makrofagi, które nie tylko kontynuują proces oczyszczania, ale także wydzielają cytokiny i czynniki wzrostu, stymulujące angiogenezę i fibroplazję. Klinicznymi objawami tej fazy są zaczerwienienie, obrzęk, ból oraz podwyższona temperatura w okolicy rany.",
Trzeci etap, faza proliferacyjna, rozpoczyna się około 3-4 dnia i może trwać do około 2?3 tygodni, w zależności od rozległości i głębokości uszkodzenia tkanek. W tej fazie kluczową rolę odgrywa tworzenie nowej tkanki, określanej jako ziarnina (tkanka ziarninowa). Fibroblasty intensywnie proliferują i syntetyzują składniki macierzy pozakomórkowej, w tym kolagen typu III, który stanowi rusztowanie dla odbudowującej się tkanki. Równocześnie zachodzi angiogeneza, czyli powstawanie nowych naczyń krwionośnych, co zapewnia odpowiednie ukrwienie i odżywienie regenerującego się obszaru. Istotnym procesem jest także epitelializacja, polegająca na migracji i namnażaniu keratynocytów z brzegów rany, prowadząca do jej stopniowego zamknięcia. W tej fazie rana ulega obkurczaniu dzięki działaniu miofibroblastów.
Ostatnim etapem jest faza remodelingu (przebudowy), która może trwać od kilku tygodni do nawet kilkunastu miesięcy. W jej trakcie dochodzi do reorganizacji i dojrzewania tkanki bliznowatej. Kolagen typu III zostaje stopniowo zastępowany bardziej wytrzymałym kolagenem typu I, a włókna kolagenowe ulegają uporządkowaniu zgodnie z liniami napięcia skóry. Zmniejsza się liczba naczyń krwionośnych, co prowadzi do blednięcia blizny. Ostatecznie tkanka bliznowata osiąga maksymalnie około 70?80% wytrzymałości mechanicznej nieuszkodzonej skóry.
Pierwsze godziny po urazie
Faza zapalna jest początkową reakcją organizmu na uszkodzenie tkanki, rozpoczynającą się natychmiast po urazie i trwającą zazwyczaj od 2 do 5 dni. W jej przebiegu dochodzi do hemostazy, czyli zatrzymania krwawienia poprzez skurcz naczyń i utworzenie skrzepu z płytek krwi. Bezpośrednio po tym następuje intensywny napływ komórek odpornościowych, głównie neutrofili, które docierają do miejsca zranienia w ciągu pierwszych 24 godzin. Zadaniem neutrofili jest fagocytoza, czyli pochłanianie i niszczenie drobnoustrojów oraz martwych komórek, co stanowi pierwszą linię obrony przed infekcją.
Po około 2-3 dniach od urazu w ranie pojawiają się makrofagi, które stopniowo zastępują neutrofile w procesie oczyszczania tkanki. Makrofagi kontynuują fagocytozę, usuwając pozostałości komórkowe, zużyte neutrofile oraz ewentualne patogeny. Pełnią one również funkcję regulatorową, uwalniając liczne cytokiny prozapalne oraz czynniki wzrostu. Jednym z mediatorów jest transformujący czynnik wzrostu beta (TGF-?), który stymuluje fibroblasty i inicjuje kolejny etap gojenia, czyli fazę proliferacyjną.
Równolegle do migracji komórek, w miejscu urazu uwalniane są mediatory zapalne, takie jak histamina i bradykinina. Substancje te powodują rozszerzenie naczyń krwionośnych (wazodylatację) oraz zwiększenie ich przepuszczalności. Klinicznie objawia się to zaczerwienieniem, obrzękiem i podwyższoną temperaturą w okolicy rany. Zwiększona przepuszczalność śródbłonka naczyniowego ułatwia migrację kolejnych komórek odpornościowych oraz białek osocza do uszkodzonej tkanki, wspierając procesy obronne i naprawcze.
Objawy początkowej reakcji organizmu
Początkowa reakcja organizmu na uraz manifestuje się czterema klasycznymi objawami stanu zapalnego: zaczerwienieniem (rubor), obrzękiem (tumor), ociepleniem (calor) oraz bólem (dolor). Zaczerwienienie i ocieplenie są bezpośrednim wynikiem lokalnego rozszerzenia naczyń krwionośnych, co prowadzi do zwiększonego przepływu krwi w uszkodzonym obszarze. Zwiększony przepływ krwi umożliwia szybkie dostarczenie do rany komórek odpornościowych, tlenu i składników odżywczych. Cały proces jest inicjowany przez mediatory chemiczne, takie jak histamina, uwalniane z komórek tucznych w odpowiedzi na uszkodzenie.
Obrzęk jest efektem zwiększonej przepuszczalności naczyń włosowatych, co pozwala na przenikanie płynu bogatego w białka z krwiobiegu do otaczających tkanek. Nagromadzony płyn wywiera mechaniczny nacisk na zakończenia nerwowe, co jest jednym z mechanizmów powstawania bólu. Ból jest dodatkowo potęgowany przez działanie mediatorów zapalnych, takich jak prostaglandyny i bradykinina, które bezpośrednio aktywują receptory bólowe. Substancje te obniżają również próg pobudliwości nocyceptorów, prowadząc do zwiększonej wrażliwości na bodźce w okolicy rany.
Charakterystyka fazy proliferacyjnej
Faza proliferacyjna rozpoczyna się około 3-5 dni po urazie i trwa do 3 tygodni, a jej celem jest wypełnienie ubytku tkankowego nowo powstałą strukturą. W tym okresie w łożysku rany formuje się ziarnina, która jest tymczasową macierzą biologiczną, stanowiącą podstawę dla odbudowy skóry właściwej. Ziarnina ma charakterystyczny, czerwony i grudkowaty wygląd, wynikający z obfitego unaczynienia powstałego w procesie angiogenezy. Główne komórki budujące ziarninę to fibroblasty, które migrują do obszaru uszkodzenia w odpowiedzi na czynniki wzrostu uwalniane w fazie zapalnej.
Fibroblasty w fazie proliferacyjnej aktywnie syntetyzują składniki macierzy zewnątrzkomórkowej, w tym kolagen typu III, glikozoaminoglikany oraz fibronektynę. Kolagen typu III, o cieńszych i mniej zorganizowanych włóknach niż kolagen typu I, zapewnia początkową wytrzymałość mechaniczną nowo powstałej tkance. Jednocześnie miofibroblasty, wyspecjalizowane formy fibroblastów, powodują obkurczanie się brzegów rany, co mechanicznie zmniejsza jej powierzchnię. Ten proces kontrakcji rany jest odpowiedzialny za zmniejszenie rozmiaru przyszłej blizny.
Równolegle do tworzenia ziarniny przebiega proces re-epitelializacji, czyli odtwarzania ciągłości naskórka. Keratynocyty z brzegów rany oraz ocalałych przydatków skóry, takich jak mieszki włosowe, migrują po powierzchni ziarniny, aby zamknąć ubytek. Proces ten jest stymulowany przez czynniki wzrostu, takie jak naskórkowy czynnik wzrostu (EGF) i transformujący czynnik wzrostu alfa (TGF-?). Po całkowitym pokryciu rany nowym naskórkiem, keratynocyty różnicują się, tworząc wielowarstwową strukturę o funkcji barierowej.
Kiedy powstaje nowa tkanka?
Nowa tkanka, określana jako ziarnina, zaczyna formować się w miejscu uszkodzenia około 3-5 dnia po urazie, bezpośrednio po zakończeniu ostrej fazy zapalnej. Jej struktura składa się z nowo utworzonych naczyń włosowatych, fibroblastów, makrofagów oraz luźnej macierzy zewnątrzkomórkowej. Głównym zadaniem ziarniny jest wypełnienie ubytku tkankowego, co tworzy podłoże dla kolejnych etapów naprawczych, takich jak naskórkowanie. Makroskopowo ziarnina ma charakterystyczny, czerwony i wilgotny wygląd z powodu gęstej sieci naczyń krwionośnych.
Aktywność fibroblastów w ziarninie prowadzi do intensywnej syntezy kolagenu typu III, który pełni funkcję tymczasowego rusztowania dla formującej się tkanki. Równolegle zachodzi proces angiogenezy, czyli tworzenia nowych naczyń krwionośnych, które dostarczają tlen i składniki odżywcze niezbędne do regeneracji. Makrofagi obecne w ziarninie nie tylko usuwają resztki komórkowe, ale również wydzielają czynniki wzrostu stymulujące proliferację komórek. Stopniowo, wraz z dojrzewaniem tkanki, ziarnina ulega przebudowie, a kolagen typu III jest zastępowany przez bardziej wytrzymały kolagen typu I.
Dojrzewanie blizny
Faza remodelingu, czyli dojrzewanie blizny, jest najdłuższym etapem gojenia, trwającym od 6 miesięcy do 2 lat, a w niektórych przypadkach dłużej. W tym okresie następuje stopniowa zamiana kolagenu typu III, charakterystycznego dla wczesnej ziarniny, na bardziej zorganizowany i wytrzymały kolagen typu I. Proces ten jest kontrolowany przez równowagę między enzymami rozkładającymi kolagen (metaloproteinazami) a ich inhibitorami. Włókna kolagenowe ulegają reorganizacji, układając się wzdłuż linii napięcia skóry.
W trakcie dojrzewania blizna zwiększa swoją wytrzymałość mechaniczną na rozciąganie, osiągając ostatecznie do 80% pierwotnej wytrzymałości zdrowej skóry. Zmniejsza się również unaczynienie w obrębie tkanki bliznowatej, co prowadzi do jej stopniowego blednięcia. Zmiana barwy z czerwonej lub różowej na odcień zbliżony do koloru skóry jest charakterystycznym elementem tego etapu. Blizna staje się także bardziej płaska i miękka w dotyku.
Na poziomie komórkowym faza remodelingu charakteryzuje się spadkiem gęstości komórek, w tym fibroblastów i miofibroblastów, co skutkuje obniżeniem tempa syntezy kolagenu. Aktywność metaboliczna w bliźnie ulega wyciszeniu, a procesy tworzenia i rozkładu macierzy zewnątrzkomórkowej osiągają stan równowagi. Zaburzenie tej równowagi w kierunku nadmiernej syntezy kolagenu może skutkować formowaniem blizn patologicznych, takich jak blizny przerostowe czy keloidy.
Jak długo trwa przebudowa kolagenu?
Przebudowa kolagenu w tkance blizny jest procesem, który może trwać od kilku miesięcy do dwóch lat, a jego czas zależy od wielkości uszkodzenia oraz indywidualnych predyspozycji organizmu. W tym okresie zachodzi dynamiczna wymiana kolagenu typu III, dominującego we wczesnej fazie gojenia, na bardziej wytrzymały mechanicznie kolagen typu I. Proces ten prowadzi do stopniowego zwiększania odporności blizny na rozciąganie. Za degradację tymczasowych włókien kolagenowych odpowiadają enzymy z grupy metaloproteinaz macierzy (MMPs).
Aktywność metaloproteinaz jest precyzyjnie regulowana przez ich naturalne inhibitory, określane jako tkankowe inhibitory metaloproteinaz (TIMPs). Zapewniają one kontrolę nad procesem rozkładu, zapobiegając nadmiernej degradacji nowo syntetyzowanych białek macierzy zewnątrzkomórkowej. Równowaga między działaniem MMPs a TIMPs bezpośrednio wpływa na ostateczną strukturę, elastyczność oraz wygląd blizny. Zaburzenie tej proporcji może prowadzić do powstawania nieprawidłowych form tkanki bliznowatej.
Kiedy blizna zmienia wygląd i blednie?
Blizna zmienia swój wygląd w miarę dojrzewania, przechodząc z fazy początkowej, charakteryzującej się zaczerwienieniem i uniesieniem, do fazy dojrzałej. Początkowe zaczerwienienie blizny, określane jako rumień, wynika ze zwiększonego unaczynienia (angiogenezy) i obecności aktywnych naczyń krwionośnych w fazie proliferacyjnej gojenia. Zwiększony przepływ krwi jest niezbędny do dostarczania tlenu i składników odżywczych dla komórek zaangażowanych w proces naprawczy. W tym okresie tkanka bliznowata może być również twarda i swędząca z powodu trwającego stanu zapalnego oraz przebudowy macierzy zewnątrzkomórkowej.
Proces blednięcia blizny jest bezpośrednim efektem stopniowego zmniejszania się gęstości naczyń krwionośnych oraz reorganizacji włókien kolagenowych. W miarę dojrzewania tkanki, naczynia krwionośne, które nie są już potrzebne do intensywnej regeneracji, ulegają apoptozie, czyli programowanej śmierci komórki. Równocześnie, nieuporządkowane włókna kolagenu typu III są stopniowo zastępowane przez bardziej zorganizowane i wytrzymałe mechanicznie włókna kolagenu typu I. Ta reorganizacja prowadzi do spłaszczenia i zmiękczenia struktury blizny, co jest klinicznym objawem jej dojrzewania.
Dojrzała blizna jest zazwyczaj jaśniejsza od otaczającej skóry, co jest skutkiem braku melanocytów, czyli komórek produkujących barwnik melaninę, w nowo powstałej tkance. Ostateczny wygląd blizny charakteryzuje się również tym, że jest ona bardziej płaska i miękka w dotyku w porównaniu do fazy początkowej. Tkanka bliznowata nie odzyskuje jednak pełnej elastyczności pierwotnej skóry z powodu odmiennej, bardziej zwartej architektury włókien kolagenowych. Ponadto, w obrębie blizny trwale zanikają struktury takie jak mieszki włosowe, gruczoły potowe i łojowe, co zaburza jej funkcje fizjologiczne.
Jakie wyróżniamy typy blizn?
Klasyfikacja medyczna wyróżnia cztery główne rodzaje blizn na podstawie ich morfologii oraz procesu gojenia: normotroficzne, przerostowe, zanikowe oraz keloidy (bliznowce). Blizny normotroficzne, określane również jako prawidłowe, stanowią finalny, pożądany efekt fizjologicznego gojenia się rany. Charakteryzują się płaską, miękką strukturą oraz kolorem zbliżonym do otaczającej, zdrowej skóry. Zakończony proces remodelingu w ich obrębie sprawia, że są elastyczne i nie powodują przykurczów.
Blizny przerostowe (hipertroficzne) powstają w wyniku nadmiernej produkcji kolagenu typu III w fazie proliferacyjnej gojenia. Klinicznie objawiają się jako uniesione ponad powierzchnię skóry, twarde i zaczerwienione zgrubienia, które jednak ściśle ograniczają się do granic pierwotnego urazu. Ten typ blizny często pojawia się w ciągu 4-8 tygodni po uszkodzeniu tkanki i może ulegać częściowej, spontanicznej regresji w ciągu kilku lat. W odróżnieniu od bliznowców, rzadko towarzyszy im ból czy świąd o dużym nasileniu.
Bliznowce, czyli keloidy, są patologiczną formą gojenia, w której produkcja kolagenu jest niekontrolowana, a tkanka bliznowata rozrasta się poza obszar rany. Mają postać twardych, guzowatych tworów, często o ciemniejszym zabarwieniu, którym towarzyszy ból lub intensywny świąd. Z kolei blizny zanikowe (atroficzne) charakteryzują się ubytkiem tkanki i tworzeniem zagłębień, co jest wynikiem niewystarczającej syntezy kolagenu. Przykładem tego rodzaju blizn są zmiany skórne pozostałe po ospie wietrznej lub ciężkich postaciach trądziku.
Co wpływa na kształtowanie się blizny?
Czynniki genetyczne, takie jak polimorfizmy w genach kodujących transformujący czynnik wzrostu beta (TGF-?), determinują indywidualną skłonność do patologicznego bliznowacenia. Predyspozycja ta jest szczególnie widoczna w przypadku keloidów, które dziesięciokrotnie częściej występują u osób o ciemniejszej pigmentacji skóry. Wiek pacjenta również modyfikuje proces gojenia; u dzieci i młodzieży obserwuje się wzmożoną aktywność fibroblastów, co przekłada się na wyższe ryzyko tworzenia blizn przerostowych. U osób w podeszłym wieku obniżona synteza kolagenu i zmniejszona elastyczność skóry skutkują powstawaniem blizn cieńszych, często zanikowych.
Lokalizacja anatomiczna rany jest bezpośrednio powiązana z ostatecznym wyglądem blizny ze względu na zróżnicowane napięcie mechaniczne skóry. Rany w obszarach o dużej ruchomości, takich jak stawy, mostek czy ramiona, są narażone na stałe rozciąganie, co stymuluje nadmierną produkcję kolagenu. Z kolei urazy w miejscach o niskim napięciu skóry, na przykład na powiekach, goją się z wytworzeniem mniej widocznej tkanki bliznowatej. Orientacja rany względem linii Langera, czyli naturalnych linii najmniejszego napięcia skóry, także wpływa na wynik gojenia; cięcia równoległe do tych linii pozostawiają cieńsze blizny.
Charakter urazu, w tym jego głębokość i mechanizm powstania, stanowi podstawowy czynnik prognostyczny dla wyglądu blizny. Rany penetrujące do warstwy siateczkowatej skóry właściwej wiążą się z wyższym ryzykiem nieprawidłowego gojenia niż uszkodzenia powierzchowne. Wystąpienie zakażenia bakteryjnego w obrębie rany wydłuża fazę zapalną, co może prowadzić do nasilonego włóknienia i gorszego efektu estetycznego. Choroby ogólnoustrojowe, takie jak cukrzyca upośledzająca mikrokrążenie, oraz niedobory żywieniowe, np. witaminy C lub cynku, zaburzają fizjologiczny przebieg naprawy tkanek.
Istotne aspekty
Faza dojrzewania blizny, trwająca od kilku miesięcy do dwóch lat, jest okresem, w którym odpowiednie postępowanie wpływa na ostateczną strukturę i wygląd tkanki. Prawidłowa pielęgnacja w tym czasie ma na celu modulowanie procesu przebudowy kolagenu oraz zapobieganie powstawaniu zrostów i przykurczów. Działania te koncentrują się na utrzymaniu optymalnego nawilżenia naskórka oraz stosowaniu kontrolowanych bodźców mechanicznych. Celem tych interwencji jest uzyskanie blizny płaskiej, elastycznej i o kolorze zbliżonym do otaczającej skóry.
Mechaniczna stymulacja blizny, realizowana poprzez regularny masaż, zwiększa jej elastyczność i przesuwalność względem głębiej położonych tkanek. Wykonywanie ruchów okrężnych lub linearnych przez kilka minut dziennie wspomaga prawidłowe ułożenie włókien kolagenowych i poprawia lokalne mikrokrążenie. Utrzymywanie odpowiedniego nawilżenia poprzez aplikację preparatów okluzyjnych, takich jak żele silikonowe, ogranicza transepidermalną utratę wody (TEWL). Stworzenie wilgotnego środowiska sprzyja aktywności enzymów odpowiedzialnych za remodelowanie macierzy zewnątrzkomórkowej.
Ochrona niedojrzałej blizny przed promieniowaniem ultrafioletowym (UV) jest niezbędna w celu prewencji hiperpigmentacji pozapalnej. Tkanka bliznowata, szczególnie w pierwszym roku po urazie, wykazuje zwiększoną wrażliwość melanocytów na promieniowanie słoneczne, co prowadzi do jej trwałego przebarwienia. Aplikacja preparatów z filtrem o wysokim wskaźniku ochrony przeciwsłonecznej, na poziomie SPF 30 lub SPF 50, stanowi podstawową metodę fotoprotekcji. Dodatkową barierę ochronną stanowią osłony fizyczne, takie jak odzież lub specjalistyczne plastry ochronne.